Проведение контроля газовой стерилизации с применением окиси этилена
Персонал лечебного учреждения должен проводить контроль стерилизации с применением физического, химического и биологического методов. Если результаты одного из видов контроля являются неудовлетворительными, цикл стерилизации считается не эффективным и загрузку признают нестерильной.
Биологические методы контроля газовой стерилизации
На рисунке приведен внешний вид биологического индикатора.

Рис. Биологический индикатор Аттест 1264
Биологические индикаторы являются единственным способом индикации гибели спор микроорганизмов. Споры Bacillus atropaeus (ранее Bacillus subtilis), используемые для контроля стерилизации окисью этилена, считаются наиболее надежным средство контроля эффективности стерилизации.
Применение биологических индикаторов
Биологические индикаторы применяются в следующих случаях:
- для рутинного контроля эффективности стерилизации;
- для квалификационных проверок стерилизатора после инсталляции, перемещения, обнаружения и устранения неисправностей;
- для контроля каждой загрузки, содержащей имплантируемые изделия;
- для периодического тестирования.
Контроль работы стерилизационной системы «Стери-Вак» и других газовых этиленоксидных стерилизаторов биологическим методом осуществляется с помощью биологических индикаторов «Аттест 1264» однократного применения.
При контроле циклов стерилизации биологические индикаторы размещают в тех же точках, что и химические индикаторы, размещая радом с максимальными термометрами в центре и на дно корзины, между упаковками, а также возле загрузочной и разгрузочной двери стерилизационной камеры.
После окончания стерилизационного цикла в биологических индикаторах нужно раздавить ампулы, чтобы питательная среда пропитала полоску со спорами, и поместить индикатор в металлический блок инкубатора «Аттест 119».
Необходимо проверять индикаторы через 8, 12, 18, 24, 48 часов после начала инкубации. Окончательный результат доступен для оценки через 48 часов инкубации. Появление желтой окраски свидетельствует о бактериальном росте (положительный результат). Отсутствие окраски свидетельствует о надежности проведенного стерилизационного цикла.
Применение современных методов контроля стерилизации с использованием ОЭ позволяет сделать этот метод низкотемпературной стерилизации эффективным и безопасным для пациентов и персонала.
Индикатор биологический автономный Аттест 1264
Индикатор биологический автономный Аттест 1264 (далее – индикатора) производства фирмы «3M» (США), применяется для контроля эффективности процесса ЭО стерилизации медицинских изделий в газовых стерилизаторах по ГОСТ ISO 11135-2017.
Индикатор предназначен для использования персоналом ЛПУ, предприятий и служб, эксплуатирующих, контролирующих и осуществляющих техническое обслуживание стерилизационного оборудования.
Индикатор соответствует требования, предъявляемым к биологическим индикаторам по ГОСТ ISO 11138, EN 866-1 и EN 866-2.
Индикатор (рис. ниже) представляет собой пластиковую пробирку с размещенной внутри стеклянной ампулой с питательной средой сине-фиолетового цвета и выпущенными спорами бактерий Bacillus atropaeus (Bacillus subtilis) в количестве 105.

Рис. Схема строения индикатора биологического автономного Аттест 1264
Пластиковая пробирка герметично закрыта зеленым колпачком, в котором имеются отверстия с бактериальным фильтром. При газовой стерилизации через отверстия с фильтром проходит удаление воздуха из пробирки и проникновение окиси этилена. В качестве фильтров используется пористый целлюлозный материал, не пропускающий микроорганизмы и их споры.
Индикатор необходимо применять как для периодического, так и текущено контроля газовой (ОЭ) стерилизации.
Индикатор предназначен для контроля эффективности стерилизации окисью этилена медицинских изделий во всех режимах, а именно: температура 25-60 °С, влажность 30-95% для 20-100% ОЭ. Индикатор не предназначен для контроля режимов паровой, воздушной, формальдегидной стерилизации.
Применение индикатора позволяет выявить неэффективную стерилизацию ОЭ медицинских изделий, обусловленную технической неисправностью стерилизаторов, нарушением правил их загрузки и эксплуатации, ошибкой в установке значений параметров или их сбоем, и тем самым уменьшить риск использования нестерильных медицинских изделий.
При работе с индикатором не потребуется специальных асептических блоков и помещений, они безопасны в использовании.
На упаковке с индикаторами указаны их наименование, срок годности, номер партии и реквизиты предприятия-изготовителя и предприятия-поставщика.
Хранить индикаторы нужно при обычных комнатных условиях, при температуре +15 °С- +30 °С и относительной влажности воздуха 35-60% без воздействия прямых солнечных лучей и паров дезинфицирующих и химических реактивов.
Индикаторы следует транспортировать в транспортной таре без воздействия атмосферных осадков при температуре +15 °С- +30 °С в и относительной влажности воздуха 35-60%.
Гарантийный срок годности индикаторов составляет 24 месяца с даты выпуска при соблюдении условий хранения и транспортировки.
Проведение и периодичность контроля биологическими индикаторами
Обязательный контроль эффективности стерилизации газовых этиленоксидных стерилизаторов с помощью индикаторов необходимо осуществлять:
- после монтажа и ремонта стерилизатора;
- во время планового периодического (ежеквартального) контроля стерилизации в процессе эксплуатации;
- при обнаружении неудовлетворительных результатов контроля физическими и химическими методами;
- при выявлении нестерильных МИ методом смыва с простерилизованных изделий.
Контроль проводит персонал организаций, осуществляющий монтаж и техническое обслуживание оборудования, или сотрудники ЛПУ, осуществляющих техническое обслуживание, или персонал организаций, контролирующих дезинфекционную и стерилизационную деятельность.
Текущий контроль эффективности газовой (ЭО) стерилизации МИ рекомендуется проводить индикаторами 1 раз в две недели. В случае стерилизации особо важных и ответственных МИ имплантируемых изделий, изделий для оперативных вмешательств с высоким риском (ВБИ) проводится контроль биологическими индикаторами каждого цикла стерилизации.
Текущий контроль должен проводить персонал, эксплуатирующий стерилизационное оборудование.
Количество биологических индикаторов, необходимых для одного испытания стерилизатора на эффективность стерилизации, зависит от объема стерилизационной камеры.
- после монтажа и ремонта стерилизатора;
- во время планового периодического (ежеквартального) контроля стерилизации в процессе эксплуатации;
- при обнаружении неудовлетворительных результатов контроля физическими и химическими методами;
- при выявлении нестерильных МИ методом смыва с простерилизованных изделий.
Контроль проводит персонал организаций, осуществляющий монтаж и техническое обслуживание оборудования, или сотрудники ЛПУ, осуществляющих техническое обслуживание, или персонал организаций, контролирующих дезинфекционную и стерилизационную деятельность.
Текущий контроль эффективности газовой (ЭО) стерилизации МИ рекомендуется проводить индикаторами 1 раз в две недели. В случае стерилизации особо важных и ответственных МИ имплантируемых изделий, изделий для оперативных вмешательств с высоким риском (ВБИ) проводится контроль биологическими индикаторами каждого цикла стерилизации.
Текущий контроль должен проводить персонал, эксплуатирующий стерилизационное оборудование.
Количество биологических индикаторов, необходимых для одного испытания стерилизатора на эффективность стерилизации, зависит от объема стерилизационной камеры.
Порядок проведения контроля эффективности стерилизации
Перед использованием индикатора следует проверит срок его годности, целостность пластиковой и стеклянной ампулы, целостность бактериальных фильтров. Индикаторы с разбитой стеклянной внутренней ампулой, или индикаторы с цветом питательной среды, отличной от сине-фиолетового (во внутренней стеклянной ампуле), использовать не разрешается.
Каждый индикатор может быть использован только однократно.
Индикатор перед закладкой в камеру стерилизатора нужно промаркировать (ставить номер стерилизатора, номер контрольной точки).
По окончании цикла стерилизации, индикатор нужно извлечь из стерилизационной камеры и совместно с одним исходным индикатором (необработанный в стерилизационном цикле) поставить в инкубатор.
Виды инкубаторов и инкубация биологического индикатора
Система Аттест предлагает 2 вида инкубаторов:
- инкубатор Attest модели 119 на 14 индикаторов;
- инкубатор Attest модели 129 на 28 индикаторов.
В камере инкубатора постоянно поддерживается заданная температура инкубации 37±2 °С.
Порядок работ по инкубации биологического индикатора
Индикатор помещают в ячейку металлического блока инкубатора нижней частью пробирки с колпачком вверх под углом 45°. При нажатии с силой на пробирку вниз ломается внутренняя стеклянная ампула с питательной средой и индикатор активизируется. При этом обязательно нужно следить, чтобы индикатор и внутренняя ампула остыли ниже температуры инкубации (пробирка должна остывать на воздухе не менее 10 минут). Во избежание попадания питательной среды на фильтр после разрушения стеклянной ампулы индикатор необходимо держать только вверх колпачком.
Порядок размещения индикатора в инкубаторе приведен на рисунке ниже
Каждый индикатор может быть использован только однократно.
Индикатор перед закладкой в камеру стерилизатора нужно промаркировать (ставить номер стерилизатора, номер контрольной точки).
По окончании цикла стерилизации, индикатор нужно извлечь из стерилизационной камеры и совместно с одним исходным индикатором (необработанный в стерилизационном цикле) поставить в инкубатор.
Виды инкубаторов и инкубация биологического индикатора
Система Аттест предлагает 2 вида инкубаторов:
- инкубатор Attest модели 119 на 14 индикаторов;
- инкубатор Attest модели 129 на 28 индикаторов.
В камере инкубатора постоянно поддерживается заданная температура инкубации 37±2 °С.
Порядок работ по инкубации биологического индикатора
Индикатор помещают в ячейку металлического блока инкубатора нижней частью пробирки с колпачком вверх под углом 45°. При нажатии с силой на пробирку вниз ломается внутренняя стеклянная ампула с питательной средой и индикатор активизируется. При этом обязательно нужно следить, чтобы индикатор и внутренняя ампула остыли ниже температуры инкубации (пробирка должна остывать на воздухе не менее 10 минут). Во избежание попадания питательной среды на фильтр после разрушения стеклянной ампулы индикатор необходимо держать только вверх колпачком.
Порядок размещения индикатора в инкубаторе приведен на рисунке ниже

При проведении инкубации нужно поместить еще один индикатор (необработанный в цикле стерилизации ЭО) из той же серии (партии) и то же даты производства, что и инкубируемый, обработанный в стерилизаторе индикатор.
Целью инкубации необработанного (исходного) индикатора является:
- контроль правильности условий инкубации;
- проверка жизнеспособности спор в индикаторах данной партии;
- проверка годности питательной среды для роста микроорганизмов данного вида.
Предварительные результаты контроля можно получить через 12-24 часа, но окончательное заключение о результатах контроля можно делать только после 48 часов инкубации.
Целью инкубации необработанного (исходного) индикатора является:
- контроль правильности условий инкубации;
- проверка жизнеспособности спор в индикаторах данной партии;
- проверка годности питательной среды для роста микроорганизмов данного вида.
Предварительные результаты контроля можно получить через 12-24 часа, но окончательное заключение о результатах контроля можно делать только после 48 часов инкубации.
Трактовка результатов инкубации биологических индикаторов
Исходная питательная среда имеет сине-фиолетовый цвет. Изменение цвета питательной среды на желтый хотя бы одного активированного индикатора, обработанного в стерилизаторе, свидетельствует о росте колонии микроорганизмов и показывает, что споры микроорганизмов при газовой (ОЭ) стерилизации не погибли и стерилизационный цикл не обеспечил необходимую эффективность стерилизации. Сохранение исходного сине-фиолетового цвета питательной среды обработанных в стерилизаторе индикаторов указывает на гибель спор микроорганизмов и на обеспечение необходимой эффективности стерилизации в контрольных точках, в которых находились индикаторы.
Для получения выводов об эффективности стерилизации трудностерилизуемых изделий индикаторы необходимо располагать в центре этих изделий, например, в центре стандартной тестовой упаковки из хлопчатобумажных простыней (по ГОСТ Р 51935-2002 и ГОСТ 31598-2012).
Результаты контроля индикаторами верны только после инкубации в случае, если контрольный индикатор (необработанный в газе) изменил свой цвет на желтый (рис).
Для получения выводов об эффективности стерилизации трудностерилизуемых изделий индикаторы необходимо располагать в центре этих изделий, например, в центре стандартной тестовой упаковки из хлопчатобумажных простыней (по ГОСТ Р 51935-2002 и ГОСТ 31598-2012).
Результаты контроля индикаторами верны только после инкубации в случае, если контрольный индикатор (необработанный в газе) изменил свой цвет на желтый (рис).

Результаты необходимо записать в журнал контроля работы газовых стерилизаторов с указанием параметров стерилизационной выдержки (температуры, время), даты контроля, номера стерилизатора, ФИО проводившего контроль, количества тестовых упаковок, количества проросших и непроросших индикаторов. Прикладываемую к каждому индикатору наклейку необходимо вклеить в журнал контроля работы газовых стерилизаторов.
При прорастании хотя бы одного биологического индикатора, обработанного в стерилизаторе, результаты контроля считаются отрицательными. При этом эксплуатацию стерилизатора приостанавливают, выясняют причину нарушения условий стерилизации, устраняют их. Эксплуатация стерилизатора разрешается только после проведения испытания стерилизатора на эффективность и повторного контроля эффективности стерилизации с помощью биологических индикаторов.
Причинами неудовлетворительной стерилизации могут быть:
- неудовлетворительное удаление воздуха из стерилизационной камеры;
- использование неправильной программы стерилизации;
- сбой параметров стерилизационного цикла;
- негерметичность стерилизационной камеры;
- нарушение правил загрузки – переуплотнение стерилизационной камеры;
- нарушение правил упаковки МИ.
Биологические индикаторы, давшие пророст перед утилизацией необходимо подвергнуть обработке ЭО в стерилизационном цикле с параметрами стерилизационной выдержки.
Инактивированные биологические индикаторы утилизируют как безопасные медицинские отходы в соответствие с принятыми в ЛПУ правилами.
При прорастании хотя бы одного биологического индикатора, обработанного в стерилизаторе, результаты контроля считаются отрицательными. При этом эксплуатацию стерилизатора приостанавливают, выясняют причину нарушения условий стерилизации, устраняют их. Эксплуатация стерилизатора разрешается только после проведения испытания стерилизатора на эффективность и повторного контроля эффективности стерилизации с помощью биологических индикаторов.
Причинами неудовлетворительной стерилизации могут быть:
- неудовлетворительное удаление воздуха из стерилизационной камеры;
- использование неправильной программы стерилизации;
- сбой параметров стерилизационного цикла;
- негерметичность стерилизационной камеры;
- нарушение правил загрузки – переуплотнение стерилизационной камеры;
- нарушение правил упаковки МИ.
Биологические индикаторы, давшие пророст перед утилизацией необходимо подвергнуть обработке ЭО в стерилизационном цикле с параметрами стерилизационной выдержки.
Инактивированные биологические индикаторы утилизируют как безопасные медицинские отходы в соответствие с принятыми в ЛПУ правилами.
Биологические индикаторы быстрого чтения для окиси этилена
Биологические индикаторы быстрого чтения для окиси этилена являются новейшей разработкой и оптимальным выбором для быстрой индикации гибли спор микроорганизмов. Они также используют в качестве тестового микроорганизма стандартные споры Bacillus Atropheus (ранее Bacillus Subtilis).
Результаты посева получают после инкубации в авторидере Аттест (рис. ниже) в течение 4-х часов при температуре 37 °С. Кроме того, дополнительный визуальный результат получают после изменения цвета индикатора и pH среды через 96 часов продолжительной инкубации. Процесс роста бактерий, производящий изменения pH среды, также вызывает изменение цвета индикатора с зеленого на желтый, указывая на проблемы процесса этиленоксидной стерилизации.
Результаты посева получают после инкубации в авторидере Аттест (рис. ниже) в течение 4-х часов при температуре 37 °С. Кроме того, дополнительный визуальный результат получают после изменения цвета индикатора и pH среды через 96 часов продолжительной инкубации. Процесс роста бактерий, производящий изменения pH среды, также вызывает изменение цвета индикатора с зеленого на желтый, указывая на проблемы процесса этиленоксидной стерилизации.
Для использования в ЛПУ биологические индикаторы должны быть простыми, недорогими, устойчивыми к внешней контаминации, предоставлять положительный результат как можно быстрее после окончания цикла, чтобы можно было произвести корректирующие действия. Так же, они должны предоставлять положительный результат только в том случае, если все критические параметры (концентрация ЭО, влажность, время, температура) адекватны, чтобы вызвать гибель резистентных микроорганизмов. Кроме того, биологический индикатор не должен быть чрезмерно резистентным, чтобы не вызвать бесполезный отзыв изделий и повторный репроцессинг.
Биологические индикаторы быстрого чтения могут быть использованы для мониторинга ЭО циклов как на чистой 100% окиси этилена, так и для смеси газов.
Биологические индикаторы быстрого чтения не тестировались для использования в смешанных циклах с углекислотой, ЭО-СО2.
Конструкция автономного биоиндикатора (а именно то, что он содержит как споры, так и питательную среду) позволяет обеспечивать простоту и удобство применения, в том числе непосредственно в ЦСО, где расположен газовый стерилизатор.
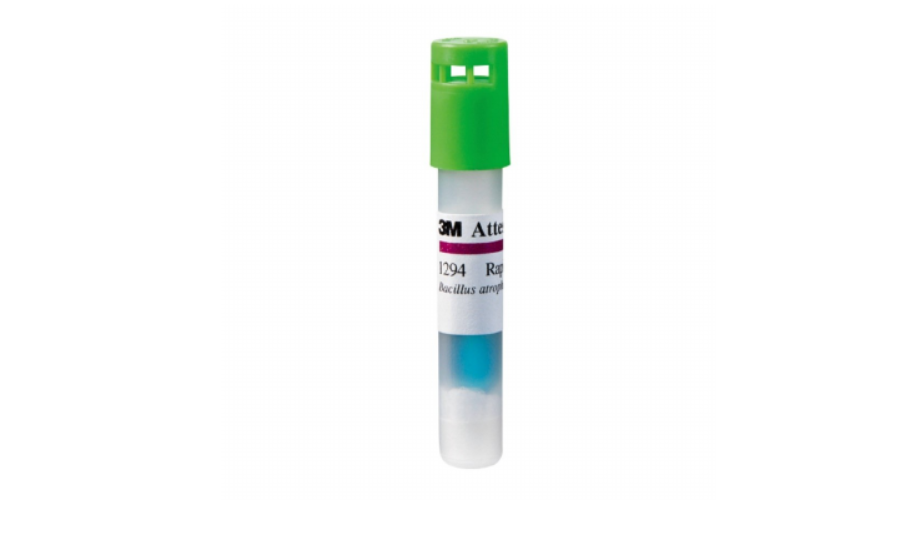
Быстродействующий биологический индикатор 3M Attest 1294 (с зеленым колпачком) предназначен для быстрого, надежного мониторинга процесса стерилизации окисью этилена при использовании совместно с автоматическим авторидером Аттест.
Быстродействующий биологический индикатор Аттест регистрирует активность природного фермента Bacillus Atropheus (ранее Bacillus Subtilis), бета-глюкозидазы, которая является одним из ферментов, участвующим в вырастании спор и нормальной вегетативной функции клеток. Автоматический ридер обнаруживает активность фермента Bacillus Atropheus путем регистрации флюоресцирующего продукта, образующегося при ферментативной деструкции субстрата, содержащегося в среде. Обнаружение фермента Bacillus Atropheus указывает на неполноту стерилизации. Окончательный вывод об отрицательной реакции биологического индикатора получают после инкубации в течение 4 часов и, в случае необходимости, продолженной инкубации в течении 96 часов.
Биоиндикаторы для быстрого чтения выпускаются двух видов.
Первый вид – это биологический индикатор Аттест 1294 быстрого чтения для окиси этилена (с зеленым колпачком, рис ниже.). Он предоставляет результат уже через 4 часа после начала инкубации, что позволяет определять ошибки стерилизации на самых ранних стадиях, практически исключая необходимость в карантинизации изделий. Это позволяет принимать решения и корректирующие действия до начала операций, что снижает риск и затраты, связанные с хирургической ВБИ.
Биологические индикаторы быстрого чтения могут быть использованы для мониторинга ЭО циклов как на чистой 100% окиси этилена, так и для смеси газов.
Биологические индикаторы быстрого чтения не тестировались для использования в смешанных циклах с углекислотой, ЭО-СО2.
Конструкция автономного биоиндикатора (а именно то, что он содержит как споры, так и питательную среду) позволяет обеспечивать простоту и удобство применения, в том числе непосредственно в ЦСО, где расположен газовый стерилизатор.
Быстродействующий биологический индикатор 3M Attest 1294 (с зеленым колпачком) предназначен для быстрого, надежного мониторинга процесса стерилизации окисью этилена при использовании совместно с автоматическим авторидером Аттест.
Быстродействующий биологический индикатор Аттест регистрирует активность природного фермента Bacillus Atropheus (ранее Bacillus Subtilis), бета-глюкозидазы, которая является одним из ферментов, участвующим в вырастании спор и нормальной вегетативной функции клеток. Автоматический ридер обнаруживает активность фермента Bacillus Atropheus путем регистрации флюоресцирующего продукта, образующегося при ферментативной деструкции субстрата, содержащегося в среде. Обнаружение фермента Bacillus Atropheus указывает на неполноту стерилизации. Окончательный вывод об отрицательной реакции биологического индикатора получают после инкубации в течение 4 часов и, в случае необходимости, продолженной инкубации в течении 96 часов.
Биоиндикаторы для быстрого чтения выпускаются двух видов.
Первый вид – это биологический индикатор Аттест 1294 быстрого чтения для окиси этилена (с зеленым колпачком, рис ниже.). Он предоставляет результат уже через 4 часа после начала инкубации, что позволяет определять ошибки стерилизации на самых ранних стадиях, практически исключая необходимость в карантинизации изделий. Это позволяет принимать решения и корректирующие действия до начала операций, что снижает риск и затраты, связанные с хирургической ВБИ.
Вторая форма выпуска – это тестовая упаковка для окиси этилена, содержащая биологический индикатор Аттест 1298 быстрого чтения (с зеленым колпачком). Она предоставляет собой готовое к применению тестовое устройство для испытания ЭО процесса, то есть устройство, предназначенное для имитации продукта и используемое для оценки проникновения стерилизующего агента в ходе цикла стерилизации. Тестовая упаковка создана специально для контроля процесса стерилизации на основе окиси этилена аналогично шприцевой тестовой упаковке, предложенной Ассоциацией ухода за медицинскими инструментами (Association foг the Advancement of Medical Instгumentation).
Результат предоставляется также через 4 часа после начала инкубации, что позволяет определить ошибки стерилизации на самых ранних стадиях, практически исключая необходимость в длительной карантинизации изделий.
Биологические индикаторы быстрого чтения 1294 и 1298 применяются ежедневно для контроля каждой загрузки газовой стерилизации окисью этилена.
С этой целью тестовая упаковка для окиси этилена, содержащая биологический индикатор Аттест 1298 быстрого чтения помещается в наиболее сложную область, в центр стерилизатора, вместе с полной загрузкой.
Данные экспериментов показывают, что чувствительность 4-х часового флюоресцентного метода составляет более 97%, на основании визуальных рост-положительных биоиндикаторов. Фактически все рост-положительные индикаторы были определены при помощи флюоресценции. Это подтверждает, что если в течении 4-х часов инкубации нет флюоресценции, то продолженная инкубация не выявит роста.
Мониторирование ЭО циклов в операционном блоке или ЦСО и получение результатов в течение 4-х часов должны обеспечить персонал возможностью элиминировать нестерильных изделий или до начала использования, или до конца операции.
В случае, если ЛПУ карантинизирует изделия в течение 4-х часов, полностью устраняется возможность использования нестерильных изделий. Также технология биологических индикаторов для быстрого чтения способна существенно повысить безопасность пациента в ЛПУ.
Результат предоставляется также через 4 часа после начала инкубации, что позволяет определить ошибки стерилизации на самых ранних стадиях, практически исключая необходимость в длительной карантинизации изделий.
Биологические индикаторы быстрого чтения 1294 и 1298 применяются ежедневно для контроля каждой загрузки газовой стерилизации окисью этилена.
С этой целью тестовая упаковка для окиси этилена, содержащая биологический индикатор Аттест 1298 быстрого чтения помещается в наиболее сложную область, в центр стерилизатора, вместе с полной загрузкой.
Данные экспериментов показывают, что чувствительность 4-х часового флюоресцентного метода составляет более 97%, на основании визуальных рост-положительных биоиндикаторов. Фактически все рост-положительные индикаторы были определены при помощи флюоресценции. Это подтверждает, что если в течении 4-х часов инкубации нет флюоресценции, то продолженная инкубация не выявит роста.
Мониторирование ЭО циклов в операционном блоке или ЦСО и получение результатов в течение 4-х часов должны обеспечить персонал возможностью элиминировать нестерильных изделий или до начала использования, или до конца операции.
В случае, если ЛПУ карантинизирует изделия в течение 4-х часов, полностью устраняется возможность использования нестерильных изделий. Также технология биологических индикаторов для быстрого чтения способна существенно повысить безопасность пациента в ЛПУ.
Использованные источники:
Корнев И.И., Логвинов Н.Л., Корнев А.И. Газовая стерилизация изделий медицинского назначения с применением окиси этилена в лечебно-профилактических учреждениях. Под общей редакцией профессора И.И. Корнева – Спб.: Человек, 2014. – 126 с.: ил.
